Vorwort
In diesem eBook wird auf weitere eBooks verwiesen. Diese sind Bestandteil meines sog. „Corobuches“.
Sie finden sie, wenn Sie auf die entsprechenden Links klicken. In diesen Kapiteln werden vor allem die Führung eines Herzkatheters und die Messungen, die man bei Katheteruntersuchung durchführt genau und sehr detailliert beschrieben.
- Für „Mein Corobuch“: Hier klicken
- Für Kapitel 10 über Messungen: Hier klicken
- Für Kapitel 12 über die Rechtsherzkatheteruntersuchung: Hier klicken
- Für Kapitel 27 über angeborene Vitien mit Shunt: Hier klicken
Morphologische und pathophysiologische Vorbemerkungen
Der offene Ductus arteriosus stellt eine Gefäßanomalie dar, die darauf beruht, daß eine im Embryonalleben bestehenden Gefäßverbindung zwischen A. pulmonalis und Aorta auch nach der Geburt bestehen bleibt.
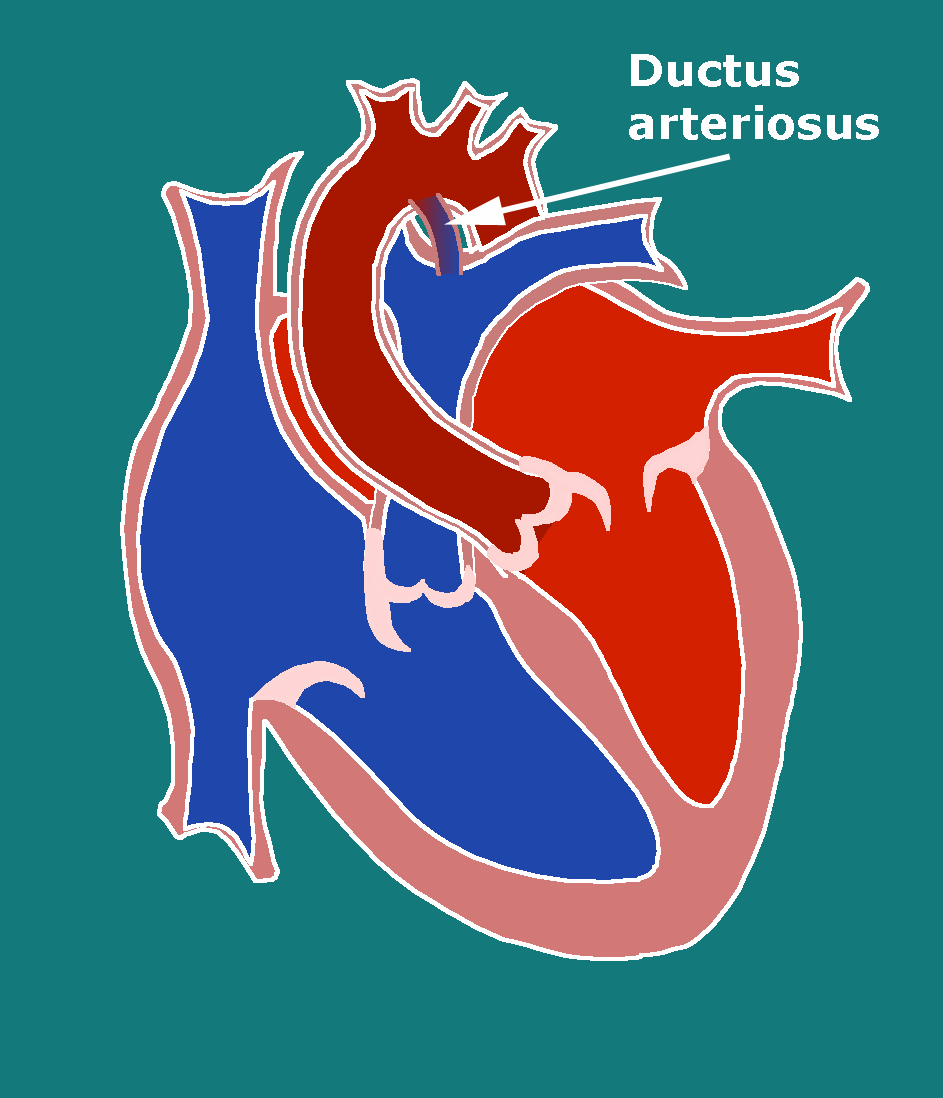
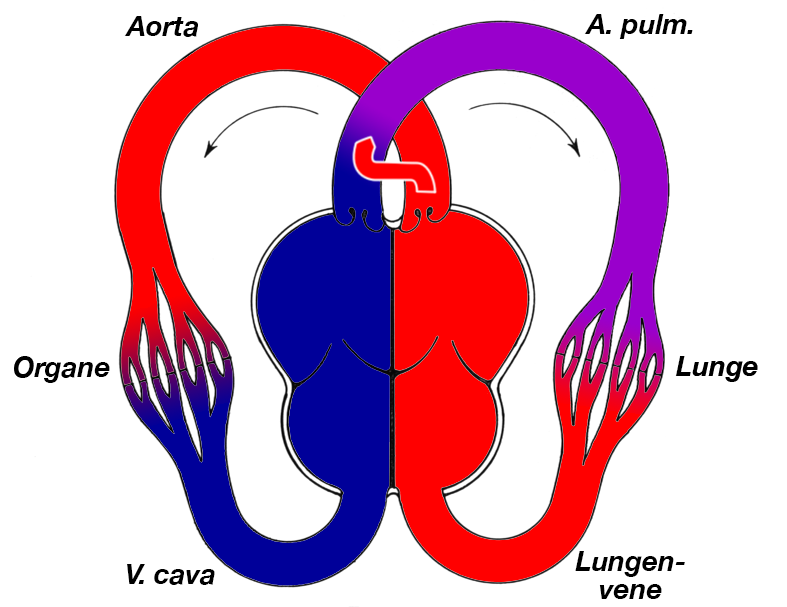
Der Ductus (Abb. 1) ist während der Intrauterinzeit ein unverzichtbarer Teil des foetalen Kreislaufes, weil er dafür sorgt, daß Blut an der noch nicht belüfteten Lunge vorbei und aus dem kleinen Kreislauf zurück in die Aorta und damit in den großen Kreislauf geleitet wird (Abb. 2).
Intrauterin bei noch funktionsfähigem Ductus unterscheidet sich der histologische Aufbau seiner Wand von demjenigen der A. pulmonalis und der Aorta. Die Wanddicke ist zwar bei allen 3 Gefäßen ähnlich, jedoch besteht die Media des Ductus nicht aus circumferentiell angeordneten elastischen Fasern wie bei Pulmonalarterie und Aorta, sondern aus glatten Muskelzellen. Wenn sich diese Muskeln kontrahieren bewirken sie eine Einengung des Lumens des Ductus und seine Verkürzung. Dieser Umstand ist beim spontanen Verschluß des Gefäßes von Bedeutung, wie Sie gleich lesen werden.
Für die Durchgängigkeit dieses lebenswichtigen Gefäßes während der gesamten Foetalzeit sind 2 wichtige Faktoren verantwortlich: Ein hämodynamischer und ein „hormoneller“ Grund.
- Solange die Lunge noch nicht belüftet ist ist der Gefäßwiderstand im Lungenkreislauf deutlich höher als derjenige im großen Kreislauf. Damit ist natürlich auch der Blutdruck in der A. pulmonalis höher als in der Aorta. Im Ductus, der ja eine Verbindung zwischen beiden Gefäßen darstellt besteht daher ein Druckgradient, der zur Folge hat, daß permanent Blut aus der A. pulmonalis in die Aorta fließt. Dies ist der hämodynamische Grund für die Durchgängigkeit des Ductus.
- Daneben gibt es noch einen „hormonellen“ Grund, der durch das Prostaglandin E2 (PGE2) vermittelt wird
PGE2 wird im Gegensatz zu Hormonen nicht zentral an einem Ort produziert und wirken auch nicht über die Blutbahn an entfernten Organen und Geweben. Es wird vielmehr an verschiedenen Stellen im Körper produziert und wirken nur dort in der direkter Umgebung seiner Entstehung.
Es ist in seiner Entstehung u.a. gekoppelt an den Sauerstoffgehalt des Blutes und der Gewebe in dem Sinne, daß es bei Hypoxie verstärkt und vermehrt gebildet wird. An diesem Mechanismus sind die Zyklooxygenase 2, eine der „extracellular-signal regulated Protein-Kinasen“ und „reaktive Sauerstoffspezies“ beteiligt.
PGE2 entfaltet seine Wirkung durch sein Andocken an die 4 Rezeptoren EP1 - EP4. Die Art seiner Wirkung hängt dabei davon ab, welchen dieser Rezeptoren es aktiviert. Der EP4-Rezeptor z.B. verursacht bei seiner Aktivierung durch PGE2 eine Gefäßdilatation. Und weil im Ductus arteriosus ganz überwiegend EP4-Rezeptoren vorhanden sind bewirkt das PGE2 hier eine Vasodilatation des Gefäßes. Dies ist der hormonelle Grund für die Durchgängigkeit des Ductus.Zum Zeitpunkt der Geburt werden die Lungen belüftet und die Funktion des Ductus ist nun nicht mehr erforderlich; im Gegenteil: Er sollte sich jetzt verschließen. Dieser Verschluß erfolgt in 2 Schritten:
- Der „funktionale“ Verschluß durch die Konstriktion der Gefäßmuskulatur in der Wand des Ductus innerhalb von 18 - 24 h nach der Geburt und der
- der “anatomische“ Verschluß des Lumens innerhalb der folgenden wenigen Tage und Wochen, wobei dieser Vorgang meistens bis zum 3. Lebensmonat abgeschlossen ist.
Bewirkt wird der Verschluß durch 2 Veränderungen, die mit dem 1. Atemzug des Neugeborenen erfolgen:
- In dem Augenblick, in dem die Lungen belüftet werden sinkt der Gefäßwiderstand im Lungenkreislauf kontinuierlich ab. Folglich sinkt damit auch der Blutdruck in der A. pulmonalis innerhalb kurzer Zeit soweit ab, daß er den Druck in der Aorta unterschreitet.
- Hierfür spielt nun das schon erwähnte PGE2 die entscheidende Rolle:
Dies hat zur Folge, daß auch der Druckgradient im Ductus abfällt und sich damit das durch den Gradienten getriebene Blutvolumen vermindert. Der entscheidende Moment ist dabei derjenige, in dem die Widerstände in kleinem und großem Kreislauf annähernd gleich sind.
Während dieser Phase besteht kein Druckgradient mehr zwischen A. pulmonalis und Aorta und der Blutfluß kommt hämodynamisch bedingt nahezu zum Erliegen. Diese „funktionale“ Verschluß des Ductus ist eine der Voraussetzungen für seinen weiteren physiologischen Verschluß.
Mit zunehmendem Sauerstoffgehalt des Blutes kommt es zu einer Konzentrationsabnahme des PGE2 im Ductus. Wenn hierdurch dessen vasodilatierende Wirkung wegfällt kommt es folglich zu einer Vasokonstriktion des Gefäßes.
Die Konstriktion des Ductus und die hieraus resultierende Verminderung seiner Durchblutung führt zur Hypoxie in seiner muskulären Media, was die Voraussetzung für seinen nachfolgenden anatomischen Verschluß ist. Die Hypoxie führt nämlich zu Untergängen glatter Muskelzellen in der Media und zur lokalen Bildung von Wachstumsfaktoren. Diese Wachstumsfaktoren stimulieren das Endothel des Ductus und führen zu dessen Verdickung. Diese führt dann zur Fibrose und damit zum definitiven Verschluß des Gefäßes; aus dem ehemals lumentragenden Ductus wird ein bindegewebiges Band, das Ligamentum arteriosum.
Für den hier beschriebenen physiologischen Verschluß des Ductus arteriosus sind somit 3 Voraussetzungen maßgebend:
- Der neuromuskuläre Apparat der Ductuswand muß intakt sein, damit sich das Gefäß muskuläre verengen kann.
- Es muß eine ausreichende Intimaproliferation im Ductus einsetzen.
- Die Phase, während der die Widerstände in kleinem und großem Kreislauf annähernd gleich groß sind muß ausreichend lange andauern, damit das PGE2 seine Wirkung auf die Intima entfalten kann.
Das Problem beim postnatal persistierenden offenen Ductus arteriosus scheint die abnorme Struktur seiner Gefäßwand. Die Media des Gefäßes besteht nämlich nicht aus glatter Muskulatur, sondern aus Kollagen- und elastischen Fasern. Hierdurch wird die muskulär bedingte Konstriktion des Ductus, eine der Grundvoraussetzungen seines Verschlusses verhindert.
Hinzu kommt, daß sich Endothel und veränderte Media nicht voneinander abgrenzen können, was wiederum die Intimaproliferation infolge der PGE2-Wirkung blockiert.
Bleibt der Ductus arteriosus nach der Geburt offen kehr sich der Blutfluß durch das Gefäß um:
Intrauterin strömte das Blut von der A. pulmonalis zur Aorta (Rechts-Links-Shunt). Bei absinkendem Blutdruck in der Lungenarterie infolge der postnataler Lungenbelüftung kommt es zur Umkehr des Druckgradienten, sodaß das Blut nun von der Aorta zur A. pulmonalis fließt und ein Links-Rechts-Shunt entsteht.
Das Ausmaß dieses Links-Rechts-Shunts ist dabei sowohl von der Weite des Ganges als auch vom Verhältnis der Widerstände in beiden Kreisläufen abhängig ist.
Der Durchmesser des Ganges beträgt meistens zwischen 0.5 und 0.7 cm, kann aber in einzelnen Fällen auch 1.0 cm übersteigen.
Aus dem Offenbleiben des Ductus arteriosus resultiert für die Aorta ein diastolischer Druckabfall als Ausdruck des Blutabstromes durch das „Leck im Windkessel“. Dies führt zu einer Überflutung des Lungenkreislaufes, zumal der linke Ventrikel versucht, die Shunt-bedingte Verminderung des Herzzeitvolumens im großen Kreislauf durch eine Zunahme seiner Auswurfleistung zu kompensieren. Es kommt also zur vermehrten Volumenarbeit des linken Ventrikels.
Trotz der starken Vergrößerung des Lungenzirkulationsvolumens ist der Druck in der Pulmonalarterie in der Mehrzahl der Fälle nicht erhöht. Bei sehr weitem Ductus kann es aber rein mechanisch bedingt (die druckreduzierende Wirkung des Ductus fehlt) zu einer Drucksteigerung in der Lungenarterie kommen.
Alleine die vermehrte Lungendurchblutung infolge des Shuntvolumens bedingt allerdings auch ohne eine pulmonalarterielle Druckerhöhung die Gefahr einer sich im Laufe der Zeit entwickelnden sekundären Gefäßschädigung der Lungen mit einer weiterer Zunahme des Strömungswiderstandes. Im Extremfall kommt es hierdurch bedingt dazu, daß der druck in der A. pulmonalis den Aortendruck übersteigt, was dann zur Shuntumkehr mit dem Auftreten einer Spätzyanose. In solchen Fällen mit pulmonaler Hypertonie kommt es zu einer Druckmehrarbeit und Hypertrophie des rechten Ventrikels.
Klinische Vorbemerkungen
Die körperliche Entwicklung und die Leistungsfähigkeit der Träger dieser Anomalie hängt im wesentlichen von der Größe des Ductus arteriosus und damit vom Shuntvolumen ab. Nur bei großem Kurzschluß und bei Drucksteigerung im Lungenkreislauf ist mit einer Beeinträchtigung der Patienten zu rechnen.
Anamnese
Beschwerden werden nur bei großen Defekten mit großen Shuntvolumina angegeben. Bei Säuglingen beobachtet man die klinischen Zeichen einer Linksherzinsuffizienz mit allgemeiner Unruhe, Tachypnoe, vermehrtem Schwitzen, Trinkschwäche, Gedeihstörungen und vermehrter Anfälligkeit für pulmonale Infekte.
Bei den etwas größeren Kindern werden Dyspnoe vor allem bei körperlichen Belastungen, später auch in Ruhe angegeben. Die körperliche Leistungsfähigkeit ist im Vergleich zu gleichaltrigen Kindern eingeschränkt.
Bei kleineren Defekten sind die Kinder beschwerdefrei und normal belastbar. Die Diagnose wird hier in der Regel zufällig z.B. bei einer Schuluntersuchung gestellt.
Klinische Untersuchung
Eine Zyanose besteht in den unkomplizierten Fällen nicht, sie tritt erst bei einer Shuntumkehr auf. Dabei ist zunächst überwiegend die untere Körperhälfte betroffen, erst später tritt eine generalisierte Zyanose auf.
Eine Voussure gehört nicht zum typischen Bild.
Verstärkte (tastbare) Herzaktionen und eine Verlagerung des Spitzenstoßes nach außen sind häufig.
Die Blutdruckamplitude ist beim größeren Ductus erhöht, es findet sich ein Pulsus celer et altus. Im Gegensatz zur Aortenklappeninsuffizienz wird die Amplitude des Blutdruckes bei körperlicher Belastung größer.
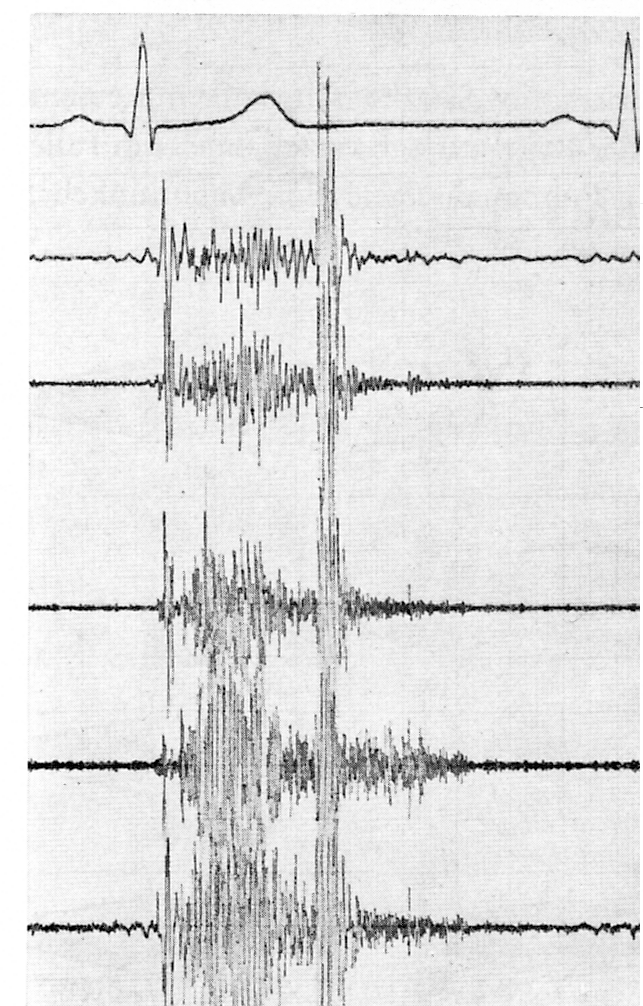
Auskultation
Der Auskultationsbefund stellt für die Diagnose des offenen Ductus arteriosus das charakteristische Symptom dar: